近日,我校科研技术中心(新安医学教育部重点实验室)胡容峰教授、陈胜麒副研究员团队在药剂学顶刊Journal of Controlled Release(中科院一区,IF=11.46)发表题为:Smart anti-vascular nanoagent induces positive feedback loop for self-augmented tumor accumulation(智能抗血管纳米制剂诱导正反馈循环,以实现自我增强的肿瘤积累)的高水平研究论文(如下图)。2020级硕士研究生杜梦婷为论文第一作者,陈胜麒副研究员和胡容峰教授为共同通讯作者,安徽中医药大学为第一作者单位。该研究获得国家自然科学基金、安徽省高校自然科学研究项目、安徽省高校协同创新项目、安徽中医药大学科技创新基金研究生项目资助。

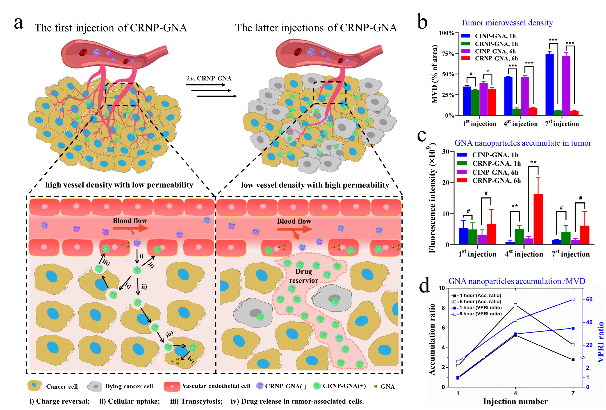
抗血管治疗疗效与药物在肿瘤中的积累之间存在困境,即抗血管疗效的发挥→肿瘤血管的减少→抗血管药物在肿瘤中的积累减少→阻碍进一步的抗血管疗效,这也是导致抗血管治疗耐药和肿瘤复发的关键因素之一。因此,如何在低血管密度的肿瘤中实现有效的药物积累是一个巨大的挑战,也是推动抗血管治疗极限的关键。在此,我们报道了一种电荷反转型新藤黄酸纳米制剂(CRNP-GNA),通过诱导“增强肿瘤血管通透性”与“改善肿瘤内药物积累”间的正反馈循环,达到自增强的药物积累、抗血管和抗肿瘤效果,最终在显著抑制肿瘤血管的同时,实现药物在肿瘤内的高效富集。相比电荷不反转型新藤黄酸纳米制剂(CINP-GNA)对照组,在多次注射给药后,CRNP-GNA组肿瘤的微血管密度从起初的几乎相等逐步降低到仅为CINP-GNA 组的7%,但瘤内的药物积累与血管的通透性和滞留指数(VPRI)却从起初的几乎相等分别提高到8.32和60倍。自增强的药物积累能够有效发挥新藤黄酸的抗血管生成、血管阻断和促凋亡等多途径抗肿瘤作用。体内研究表明,CRNP-GNA组的6只荷瘤小鼠中有5只被完全治愈。这项工作为解决抗血管治疗疗效发挥与肿瘤内药物积累之间的困境提供了一种新的策略,有望突破抗血管治疗的疗效极限。
原文链接:https://doi.org/10.1016/j.jconrel.2023.03.021
(陈胜麒/文图 李庆林/审核)